Solución Problema 1 de la Ley de Charles
Vamos a resolver el ejercicio propuesto para reforzar los conocimientos adquiridos en el tema de La Ley de Charles en el área de la teoría cinética de los gases, con este ejemplo resuelto el alumno podrá corroborar su respuesta y verificar si ha llegado al mismo resultado. ??
Nivel de Dificultad: ⭐⭐
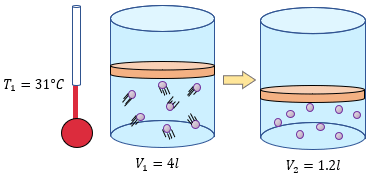
[alert-note]Problema 3.- Una masa determinada de nitrógeno gaseoso ocupa un volumen de 4 litros a una temperatura de 31°C y a una presión de una atmósfera, calcular su temperatura absoluta si el volumen que ocupa es de 1.2 litros a la misma presión [/alert-note]
Solución:
La solución del problema es muy sencillo, porque prácticamente contamos con las tres variables importantes en la ley de charles, primero nos proporcionar un volumen de 4 litros a una temperatura de 31°C estos datos son en condiciones iniciales, tanto el volumen como la temperatura, y después nos proporciona un volumen final de 1.2 litros, y es claro que lo que nos hace falta calcular es sin duda, la temperatura final.
- Obtener la temperatura final
Datos:
$ \displaystyle {{V}_{1}}=4l$
$ \displaystyle {{V}_{2}}=1.2l$
$ \displaystyle {{T}_{1}}=31{}^\circ C+273=304K$
a) Obtener la temperatura final
Recordemos que nuestra ley de charles tiene por fórmula la siguiente igualdad:
$ \displaystyle \frac{{{V}_{1}}}{{{T}_{1}}}=\frac{{{V}_{2}}}{{{T}_{2}}}$
Como la incógnita es la temperatura final, es decir T2, entonces despejamos:
$ \displaystyle {{T}_{2}}=\frac{{{V}_{2}}{{T}_{1}}}{{{V}_{1}}}$
Sustituyendo nuestros datos en la fórmula:
$ \displaystyle {{T}_{2}}=\frac{{{V}_{2}}{{T}_{1}}}{{{V}_{1}}}=\frac{\left( 1.2l \right)\left( 304K \right)}{4l}=91.2K$
Es decir que nuestra temperatura final, es de 91.2 K , recordar que la escala debe ser absoluta.
Solución:
$ \displaystyle {{T}_{2}}=91.2K$
