Solución Problema 2 de la Ley de Charles
En este segundo ejercicio resuelto, nuevamente vamos a reforzar los conocimientos adquiridos en el tema de La Ley de Charles en el área de la teoría cinética de los gases, con este ejemplo resuelto, el alumno podrá corroborar su respuesta y verificar si ha llegado al mismo resultado. ??
Nivel de Dificultad: ⭐⭐
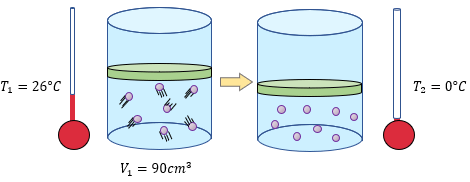
[alert-note]Problema 4.- Se tiene un gas a una temperatura de 26°C y con un volumen de 90cm³ a una presión de 760 mm de Hg, ¿Qué volumen ocupará este gas a una temperatura de 0°C, si la presión permanece constante? [/alert-note]
Solución:
Si leemos el problema encontraremos la forma de solución muy rápido, porque nos proporcionan las condiciones iniciales tanto de la temperatura como del volumen, y todo ocurre a una presión de 760 mm de Hg, esto es obvio puesto que se trata de la ley de charles. Ahora posteriormente nos proporcionan la temperatura final a 0°C, y nos piden obtener el volumen final, entonces sabemos que el volumen final es la incógnita.
- Obtener el volumen final del gas
Datos:
$ \displaystyle {{T}_{1}}=26{}^\circ C+273=299K$
$ \displaystyle {{T}_{2}}=0{}^\circ C+273=273K$
$ \displaystyle {{V}_{1}}=90c{{m}^{3}}$
a) Obtener el volumen final
Recordemos que nuestra ley de charles tiene por fórmula la siguiente igualdad:
$ \displaystyle \frac{{{V}_{1}}}{{{T}_{1}}}=\frac{{{V}_{2}}}{{{T}_{2}}}$
Como la incógnita es el volumen final, es decir V2, entonces despejamos:
$ \displaystyle {{V}_{2}}=\frac{{{V}_{1}}{{T}_{2}}}{{{T}_{1}}}$
Sustituyendo nuestros datos en la fórmula:
$ \displaystyle {{V}_{2}}=\frac{{{V}_{1}}{{T}_{2}}}{{{T}_{1}}}=\frac{\left( 90c{{m}^{3}} \right)\left( 273K \right)}{299K}=82.17c{{m}^{3}}$
Por lo que el volumen final es de 82.17cm³
Resultado:
$ \displaystyle {{V}_{2}}=82.17c{{m}^{3}}$
