Solución Problema 3 de la Ley de Boyle - Mariotte
Con este tercer problema de La Ley de Boyle - Mariotte el alumno finalmente refuerza el uso de la fórmula utilizando los diversos despejes de la fórmula, ir viendo las diversas variables que se pueden obtener a través de la fórmula de la ley de Boyle-Mariotte y que resuelve todo tipo de problemas que se puede encontrar en algún examen o tarea. ??
ivel de Dificultad: ⭐⭐
[alert-note]Problema 5.- Un gas recibe una presión de 2 atmósferas y ocupa un volumen de 125 cm³, calcular la presión que debe soportar para que su volumen sea de 95 cm³ [/alert-note]
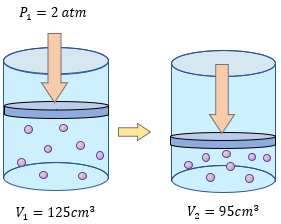
Solución:
Nuevamente este tipo de problema es un ejercicio muy fácil de resolver, pues nos proporcionan las condiciones iniciales tanto de la presión como del volumen, y sabemos nosotros que esto ocurre cuando la temperatura se mantiene constante (Esto es por la ley de Boyle - Mariotte), o también conocido como proceso isotérmico. Basándonos en los datos del problema, entonces pasemos a resolver el ejercicio.
- Obtener la presión final del gas
Datos:
$ \displaystyle {{P}_{1}}=2atm$
$ \displaystyle {{V}_{1}}=125c{{m}^{3}}$
$ \displaystyle {{V}_{2}}=95c{{m}^{3}}$
a) Obtener la presión final del gas
Recordemos que nuestra ley de Boyle - Mariotte tiene por fórmula la siguiente igualdad:
$ \displaystyle {{P}_{1}}{{V}_{1}}={{P}_{2}}{{V}_{2}}$
Como la incógnita es la presión final P2, entonces despejamos:
$ \displaystyle {{P}_{2}}=\frac{{{P}_{1}}{{V}_{1}}}{{{V}_{2}}}$
Ahora sustituimos nuestros datos en la fórmula.
$ \displaystyle {{P}_{2}}=\frac{{{P}_{1}}{{V}_{1}}}{{{V}_{2}}}=\frac{\left( 2atm \right)\left( 125c{{m}^{3}} \right)}{95c{{m}^{3}}}=2.63atm$
Es decir que ahora tenemos 2.63 atmósferas de presión final
Resultado:
$ \displaystyle {{P}_{2}}=2.63atm$
