¿Qué son los isótopos? y Ejemplos
A menudo en Química, nos topamos con algunos términos con los cuales debemos familiarizarnos, uno de ellos sin duda, son los isótopos.
Los isótopos son átomos con el mismo número de protones , pero diferentes números de neutrones . En otras palabras, tienen diferentes pesos atómicos. Los isótopos son formas diferentes de un solo elemento.
Se tiene idea que existen cerca de 275 isótopos de los 81 elementos estables. Y qué además hay más de 800 isótopos radiactivos, algunos de los cuales son naturales y otros sintéticos. Cada elemento en la tabla periódica tiene múltiples formas de isótopos. ¡Interesante! ¿no? ?
Las propiedades químicas de los isótopos de un solo elemento tienden a ser casi idénticas. Pero la excepción se encuentra en los isótopos de hidrógeno ya que el número de neutrones tiene un efecto tan significativo e importante en el tamaño del núcleo de hidrógeno. Las propiedades físicas de los isótopos son diferentes entre sí ya que estas propiedades a menudo dependen de la masa. Esta diferencia puede usarse para separar isótopos de un elemento entre sí mediante el uso de destilación fraccionada y difusión.
Con la excepción del hidrógeno, los isótopos más abundantes de los elementos naturales tienen la misma cantidad de protones y neutrones. La forma más abundante de hidrógeno es protium, que tiene un protón y ningún neutrón.
¿Cuál es la notación de los Isótopos?
Hay una forma muy común de indicar los isótopos:
Iniciando por enumerar el número masivo de un elemento después de su nombre o símbolo de elemento. Por ejemplo, un isótopo con 6 protones y 6 neutrones es carbono-12 o C-12. Un isótopo con 6 protones y 7 neutrones es carbono-13 o C-16. Tenga en cuenta que el número de masa de dos isótopos puede ser el mismo, a pesar de que son elementos diferentes. Por ejemplo, podrías tener carbono-14 y nitrógeno-14.
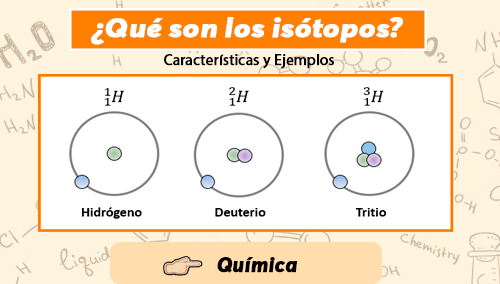
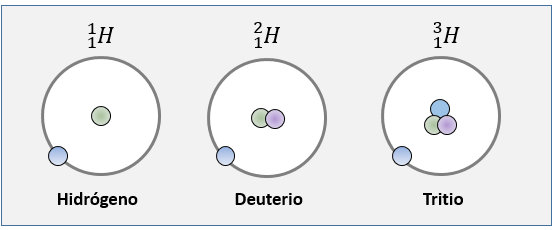
El número de masa se puede dar en el lado superior izquierdo de un símbolo de elemento. (Técnicamente, el número de masa y el número atómico se deben apilar uno al otro, pero no siempre se alinean en una computadora.) Por ejemplo, los isótopos de hidrógeno se pueden escribir:
$\displaystyle {}_{1}^{1}H,{}_{1}^{2}H,{}_{1}^{3}H$
Ejemplos de isótopos
▶️ El carbono 12 y el carbono 14 son ambos isótopos de carbono, uno con 6 neutrones y uno con 8 neutrones (ambos con 6 protones).
▶️ El carbono 12 es un isótopo estable, mientras que el carbono 14 es un isótopo radiactivo (también conocido como radioisótopo).
▶️ El uranio-235 y el uranio-238 ocurren naturalmente en la corteza terrestre. Ambos tienen largas vidas medias. El uranio-234 se forma como un producto de descomposición.
Origen e historia de la palabra isótopo
Curiosamente el término "isótopo" fue introducido por el químico británico Frederick Soddy en 1913, según lo recomendado por Margaret Todd. La palabra isótopo significa "tener el mismo lugar" de las palabras griegas isos "igual" (iso-) + topos "lugar". Los isótopos ocupan el mismo lugar en la tabla periódica, aunque los isótopos de un elemento tienen diferentes pesos atómicos.
Isótopos padre e hijos
Cuando los radioisótopos sufren desintegración radiactiva, el isótopo inicial puede ser diferente del isótopo resultante. El isótopo inicial se llama isótopo padre, mientras que los átomos producidos por la reacción se llaman isótopos hijos. Puede haber más de un tipo de isótopo secundario.
Como ejemplo, cuando el U-238 se descompone en Th-234, el átomo de uranio es el isótopo padre, mientras que el átomo de torio es el isótopo hijo.
Los isótopos radiactivos estables
La mayoría de los isótopos estables no se descomponen radiactivamente, pero algunos lo hacen.
Si un isótopo sufre desintegración radiactiva muy, muy lentamente, puede denominarse estable. Un ejemplo es bismuto-209. Bismuto-209 es un isótopo radioactivo estable que experimenta decaimiento alfa, pero tiene una vida media de 1.9 x 10^19 años (que es más de un billón de veces más larga que la edad estimada del universo). Telurio-128 sufre una desintegración beta con una vida media estimada en 7.7 x 10^24 años!
Puntos Importantes sobre los Isótopos
✅ Los isótopos son muestras de un elemento con diferentes números de neutrones en sus átomos.
✅ La cantidad de protones para diferentes isótopos de un elemento no cambia.
✅ No todos los isótopos son radiactivos. Los isótopos estables o nunca se descomponen o decaen muy lentamente. Los isótopos radiactivos sufren deterioro.
✅Cuando un isótopo se descompone, el material de partida es el isótopo padre. El material resultante es el isótopo hijo.
¿Te gustó este contenido?
Únete a nuestra comunidad en WhatsApp o Telegram para recibir nuevos proyectos, tutoriales y noticias exclusivas.
Deja una respuesta

Estos temas te pueden interesar