Solución Problema 1 de la Primera Ley de la Termodinámica
En este ejemplo de los problemas resueltos para ejercicios de práctica del tema de La primera ley de la termodinámica, es importante tener en cuenta el uso correcto de la fórmula, es por eso que se realizan los ejercicios paso a paso con su solución correspondiente. Recuerde que con este tipo de ejemplos el alumno podrá corroborar su respuesta y verificar si ha llegado al mismo resultado. ??
Nivel de Dificultad: ⭐⭐
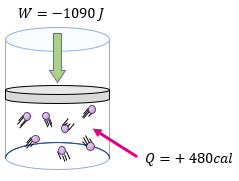
[alert-note]Problema 3.- ¿Cuál será la variación de la energía interna en un sistema que recibe 480 calorías y se le aplica un trabajo de 1090 Joules? [/alert-note]
Solución:
El problema es muy sencillo de interpretar, recordar que la variación de energía interna en un sistema es equivalente a la diferencia entre calor absorbido y el trabajo realizado. Para ello tenemos que colocar nuestra fórmula, y convertir las calorías a Joules.
- Obtener la variación de energía interna
Datos:
$ \displaystyle Q=480cal$
$ \displaystyle W=-1090J$
Nota: Hemos colocado negativo el trabajo, porque se le está aplicando trabajo al sistema.
a) Obtener la variación de energía interna
Primeramente vamos a convertir las calorías a Joules, haciendo uso de nuestro factor de conversión.
$ \displaystyle 480cal\left( \frac{4.2J}{1cal} \right)=2016J$
Tenemos nuestra fórmula:
$ \displaystyle \Delta U=Q-W$
Sustituyendo nuestros datos en la fórmula, obtenemos:
$ \displaystyle \Delta U=Q-W=2016J-\left( -1090J \right)=2016J+1090J=3106J$
Por lo que la variación de energía interna es de 3106 Joules
Solución:
$ \displaystyle \Delta U=3106J$
