Solución Problema 3 de la Primera Ley de la Termodinámica
Con este último problema de La primera ley de la termodinámica, el alumno finalmente refuerza el uso de la fórmula utilizando los despejes de la fórmula, ir viendo las diversas variables que se pueden obtener a través de la fórmula de la primera ley de la termodinámica y que resuelve todo tipo de problemas que se puede encontrar en algún examen o tarea. ??
Nivel de Dificultad: ⭐⭐⭐
Solución:
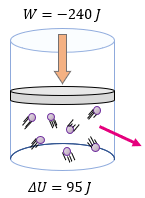
Los problemas de la primera ley de la termodinámica, requieren de mucho análisis en leer correctamente el enunciado. En este problema vemos como el sistema recibe un trabajo e inmediatamente vemos el signo negativo, lo que es correcto. Posteriormente vemos que nos dice que sufre una variación interna de 95 Joules, entonces para poder determinar la cantidad de calor en el proceso tenemos que aplicar nuestra fórmula, pero primero recopilemos los datos.
Datos:
$ \displaystyle W=-240J$
$ \displaystyle \Delta U=90J$
a) Obtener la cantidad de calor en el proceso
De la fórmula tenemos lo siguiente:
$ \displaystyle \Delta U=Q-W$
Despejando a Q
$ \displaystyle Q=\Delta U+W$
Sustituyendo nuestros datos en la fórmula, obtenemos:
$ \displaystyle Q=\Delta U+W=95J+\left( -240J \right)=-145J$
Es decir que tenemos de calor -145 Joules
Nota: El signo negativo nos indica que el sistema cede calor a los alrededores. La energía interna es positiva, porque se realizó un trabajo sobre él.
Respuesta:
$ \displaystyle Q=-145J$
