Calor Específico - Ejercicios Resueltos
Uno de los temas más destacados e importantes en calorimetría es el tema de Calor Específico, pero antes de hablar sobre el calor específico necesitamos conocer sobre el Calor Sensible y el Calor Latente, finalmente después de comprender estos términos, podremos resolver ejercicios o problemas de este tema, y adicionalmente resolveremos más ejercicios propuestos.
¿Qué es el calor sensible y el calor latente?
Cuando un cuerpo recibe o cede cierta cantidad de energía térmica, podemos observar, como consecuencia, una variación de su temperatura o un cambio en su estado físico.
La variación de temperatura corresponde a una variación en el estado de agitación de las partículas del cuerpo. En este caso, la energía térmica transferida se denomina calor sensible. El cambio de estado físico corresponde a un cambio en el estado de agregación de las partículas del cuerpo, haciendo que un sólido, por ejemplo, se transforme en líquido. La energía térmica responsable de los cambios de estado se denomina calor latente.

También es muy importante que quede bien claro la diferencia entre calor y temperatura. Calor es la denominación que damos a la energía térmica cuando, ella se encuentra transitando entre dos lugares de diferentes temperaturas. La temperatura es el estado termodinámico de un cuerpo que asociamos al nivel medio de agitación de sus partículas.

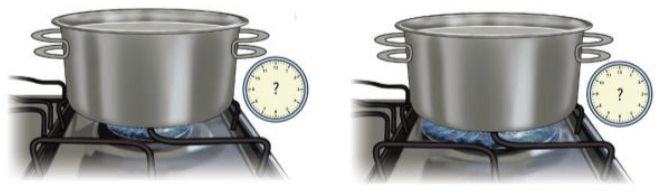
Si vemos la imagen, nos daremos cuenta de lo siguiente. La energía térmica suministrada por la llama de la estufa se utilizó inicialmente para calentar la tetera y el agua. Cuando ocurre la ebullición, observamos vapor de agua saliendo por el pico de la caldera. Este vapor es parte del agua que pasó al estado gaseoso.
¿Qué es el Calor Específico?
Para entender al Calor Específico, es importante analizar muchos casos y situaciones. Para ello lo analizaremos poco a poco.
El efecto más claro para entender este fenómeno es el siguiente, ocurre cuando la variación de temperatura de un objeto se le suministra o retira energía térmica, o sea, cuando lo calentamos o lo enfriamos. Si colocamos una olla con agua en una estufa encendida, su temperatura aumenta. Si la colocamos dentro de un refrigerador o nevera, su temperatura disminuye. ¿Pero de qué dependen estas variaciones de temperatura? Es de eso que trataremos en este artículo.
Imagine las siguientes situaciones:
Caso 1:
Tenemos dos ollas, una de hierro y otra de vidrio, conteniendo la misma cantidad de agua, se apoyan en dos quemadores de estufa diferentes. ¿Usted cree que habrá diferencia de temperaturas después de un mismo intervalo de tiempo?

Caso 2:
Dos ollas idénticas, que contengan la misma cantidad de agua, se colocan al mismo tiempo en quemadores de estufas distintas, una con la llama "baja" y la otra con la llama "alta". Usted cree que ¿habrá diferencia en el tiempo para hervir el agua?
Caso 3:
Nuevamente, tenemos dos ollas y ambas son idénticas, una conteniendo 1 litro de agua y la otra 1/2 litro, se colocan en quemadores de estufas distintas. ¿Crees que una de ellas se hervirá primero que la otra?

Las comparaciones de los casos anteriores muestran que la elevación de temperatura de un cuerpo depende del material del que está hecho (Caso 1), también depende de la cantidad de calor suministrada (Caso 2) y de la cantidad de materia del cuerpo (Caso 3). Lo mismo ocurriría en caso del enfriamiento.
[alert-warning]La característica que depende del material o de la sustancia que se hace el objeto se denomina calor específico.[/alert-warning]
En cuanto al calor específico, nos da a entender cuando un material es más difícil tanto de calentar o enfriar, o sea, menor es su variación de temperatura cuando recibe o pierde una misma cantidad de calor o energía térmica. Podemos pensar en el calor específico como una medida de "resistencia" de una sustancia a cambiar de temperatura cuando cambio el calor.
En la primera situación, la olla de hierro alcanza una temperatura más elevada que la de vidrio porque el hierro tiene menor calor específico que el vidrio.
Se define calor específico (ce) como la cantidad de calor que necesita un gramo de una sustancia para elevar su temperatura a un grado centígrado. La unidad de medida del calor específico más comúnmente utilizada es cal / g ° C.
Tabla de Calores Específicos
De esta tabla, es posible concluir que la variación de temperatura de un cuerpo, al intercambiar cierta cantidad de energía térmica, depende del material de que está constituido dicho cuerpo (calor específico) y de su masa.
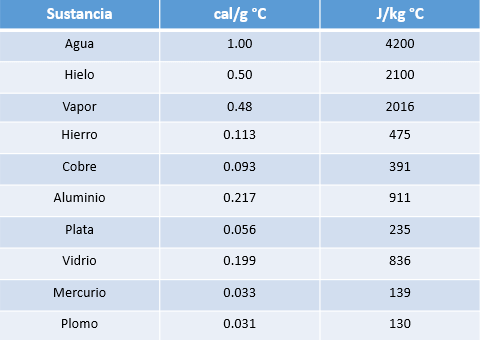
Podemos observar que el agua posee mayor calor específico, por lo que es más difícil de calentar.
Fórmula del Calor Específico
Matemáticamente expresamos al calor específico de la siguiente forma:
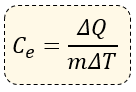
Dónde:
ΔQ = Incremento de Calor (se mide en calorías)
ΔT = Incremento de Temperatura (se mide en °C)
m = Masa (se mide en gramos)
En algunas ocasiones podemos encontrarnos la fórmula de la Capacidad Calorífica que es de donde proviene la fórmula del calor específico.
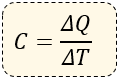
Dónde:
C = Capacidad calorífica (cal/°C)
ΔQ = Incremento de Calor (se mide en calorías)
ΔT = Incremento de Temperatura (se mide en °C)
Ejercicios Resueltos de Calor Específico
Para entender mucho mejor el tema de Calor Específico, veamos la solución de los siguientes problemas.
Solución:
El ejercicio es muy fácil de resolver, pues se cuenta con 600 gramos de hierro que inicialmente posee una temperatura de 19°C, y que se le suministra una cantidad de 1300 calorías, finalmente nos pide calcular la temperatura final, pero no olvidemos que se trata del calor específico del hierro. Así que retomando los datos tenemos.
Datos:
$\displaystyle C{{e}_{Fe}}=0.113\frac{cal}{g{}^\circ C}$
$\displaystyle m=600g$
$\displaystyle {{T}_{0}}=19{}^\circ C$
$\displaystyle \Delta Q=1300cal$
a) Obtener la temperatura final
Tenemos la fórmula del calor específico:
$\displaystyle {{C}_{e}}=\frac{\Delta Q}{m\Delta T}$
Despejando a la temperatura:
$\displaystyle \Delta T=\frac{\Delta Q}{m{{C}_{e}}}$
La variación de temperatura la podemos escribir de la siguiente manera:
$\displaystyle {{T}_{f}}-{{T}_{0}}=\frac{\Delta Q}{m{{C}_{e}}}$
Despejando a la temperatura final "Tf"
$\displaystyle {{T}_{f}}=\frac{\Delta Q}{m{{C}_{e}}}+{{T}_{0}}$
Ahora si podemos sustituir nuestros datos en la fórmula, de la siguiente forma:
$\displaystyle {{T}_{f}}=\frac{\Delta Q}{m{{C}_{e}}}+{{T}_{0}}=\frac{1300cal}{\left( 600g \right)\left( 0.113\frac{cal}{g{}^\circ C} \right)}+19{}^\circ C$
Realizando la multiplicación del denominador, obtenemos.
$ \displaystyle {{T}_{f}}=\frac{1300cal}{67.8\frac{cal}{{}^\circ C}}+{{19}^{{}^\circ }}C$
Dividiendo:
$\displaystyle {{T}_{f}}=19.17{}^\circ C+{{19}^{{}^\circ }}C$
Sumando:
$\displaystyle {{T}_{f}}=19.17{}^\circ C+{{19}^{{}^\circ }}C=38.17{}^\circ C$
Por lo que el resultado de la temperatura final es de 38.17°C
Solución:
A diferencia del primer problema, vemos que en este problema nos piden encontrar la cantidad de calor necesaria para elevar la temperatura de 24 kg de plata de 31°C hasta 110°C, pero también debemos de tener en cuenta que se trata de una barra de plata. No olvide convertir la masa en gramos.
Datos:
$\displaystyle m=24kg\left( \frac{1000g}{1kg} \right)=24000g$
$\displaystyle {{T}_{0}}=31{}^\circ C$
$\displaystyle {{T}_{f}}=110{}^\circ C$
$\displaystyle C{{e}_{Ag}}=0.056\frac{cal}{g{}^\circ C}$
a) Obteniendo la cantidad de calor para la barra de Plata
De la fórmula de calor específico tenemos:
$\displaystyle {{C}_{e}}=\frac{\Delta Q}{m\Delta T}$
Como el problema nos pide encontrar la cantidad de calor, la vamos a despejar.
$\displaystyle \Delta Q=m{{C}_{e}}\Delta T$
A la temperatura también la podemos escribir de esta forma:
$\displaystyle \Delta Q=m{{C}_{e}}\left( {{T}_{f}}-{{T}_{0}} \right)$
Ahora si podemos sustituir nuestros datos en la fórmula:
$\displaystyle \Delta Q=\left( 24000g \right)\left( 0.056\frac{cal}{{{g}^{{}^\circ }}C} \right)\left( {{110}^{{}^\circ }}C-{{31}^{{}^\circ }}C \right)$
Realizando la resta de temperaturas:
$\displaystyle \Delta Q=\left( 24000g \right)\left( 0.056\frac{cal}{{{g}^{{}^\circ }}C} \right)\left( {{79}^{{}^\circ }}C \right)$
Multiplicando las unidades, obtenemos:
$\displaystyle \Delta Q=\left( 24000g \right)\left( 0.056\frac{cal}{{{g}^{{}^\circ }}C} \right)\left( {{79}^{{}^\circ }}C \right)=106176cal$
Esto nos da un total de 106176 calorías para que ocurra todo el proceso que nos pide el problema.
Solución:
Al igual que el problema anterior, en este problema nos pide calcular la cantidad de calor, solo que este calor no se suministra sino que es un calor que se cede al ambiente porque la temperatura desciende de 130°C hasta los 10°C. El material que es sometido se trata de la plata, por lo tanto hay que tener en cuenta su calor específico.
Datos:
$\displaystyle m=5200g$
$\displaystyle {{T}_{0}}=130{}^\circ C$
$\displaystyle {{T}_{f}}=10{}^\circ C$
$\displaystyle C{{e}_{Ag}}=0.056\frac{cal}{g{}^\circ C}$
a) Obtener la cantidad de calor cedido
Aplicamos la fórmula del calor específico, pero recordemos que en el problema anterior ya hemos despejado a la variable ΔQ, esto es:
$ \displaystyle \Delta Q=m{{C}_{e}}\Delta T$
Qué también la podemos escribir de la siguiente manera:
$\displaystyle \Delta Q=m{{C}_{e}}\left( {{T}_{f}}-{{T}_{0}} \right)$
Sustituyendo los datos en la fórmula:
$\displaystyle \Delta Q=m{{C}_{e}}\left( {{T}_{f}}-{{T}_{0}} \right)=\left( 5200g \right)\left( 0.056\frac{cal}{{{g}^{{}^\circ }}C} \right)\left( 10{}^\circ C-130{}^\circ C \right)$
Resolviendo la diferencia de temperaturas:
$\displaystyle \Delta Q=\left( 5200g \right)\left( 0.056\frac{cal}{{{g}^{{}^\circ }}C} \right)\left( -120{}^\circ C \right)$
Multiplicando, finalmente obtenemos:
$\displaystyle \Delta Q=-34944cal$
Lo que es un valor de -34,944 calorías
Nota: El signo negativo (-) que hemos obtenido en el resultado, nos indica la disminución de la temperatura puesto que el cuerpo empezó a ceder calor al ambiente.
Ejercicios Para Practicar de Calor Específico
Ahora es momento de practicar con algunos ejemplos y problemas propuestos. Cada uno tiene su propia solución para verificar si ha llegado al resultado correcto. ??
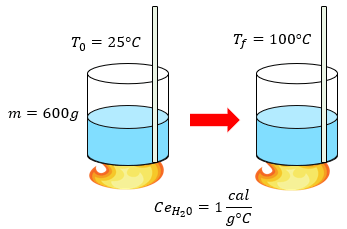
[alert-note] Problema 4.- ¿Qué cantidad de calor se necesita suministrar a 600 gramos de agua para que eleve su temperatura de 25°C a 100°C? [/alert-note]
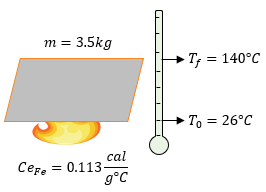
[alert-note] Problema 5.- ¿Cuántas calorías se deben suministrar para que un pedazo de metal de hierro de 3.5kg eleve su temperatura de 26°C a 140°C? [/alert-note]
[alert-note] Problema 6.- Determine el calor específico de una pieza de 720.325 gramos que requiere 2300 calorias para elevar su temperatura de 37°C a 140°C. Consulte el cuadro de calores específicos para identificar que tipo de sustancia se trata. [/alert-note]
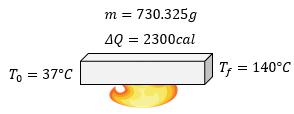
Examen de Calor Específico
Ahora que aprendiste a resolver los ejercicios, es necesario que practiquemos el siguiente examen. ¡Suerte!
Cargando examen...
¿Te gustó este contenido?
Únete a nuestra comunidad en WhatsApp o Telegram para recibir nuevos proyectos, tutoriales y noticias exclusivas.
-
Super super loca kokaa mucha infomation 😒
★★★★★
-
Muy bueno
★★★★★
-
Quisiera que me ayudaran a resolver el problema que me dise 700 gramos de hierro se encuentra a una temperatura de 19°c cuál será su temperatura final si se le suministran 1200 calorías
-
hola
-
Estos ejercicios me sirvieron para entender del todo esta parte, muchas graciasss por explicarlo tan detallado ???
-
Estos ejercicios me sirvieron para entender del todo esta parte, muchas graciasss por explicarlo tan detallado ??
-
Tremenda explicación tengo todo claro?
-
se desea fundir 30 gramos de plomo y tiene un calor especfico de 0.031 calorias sobre grados celsius. ¿cual es su temperatura que se debe suministrar si de calor tiene 375.8calorias?
me ayudan a resolverlo.
-
1.- Se calienta una pieza de cobre de 120 gramos a 200 ºC. Luego se sumerge en un recipiente que contiene 150 gramos agua a 20 ºC. ¿Cuál será la temperatura final del sistema después de establecerse el equilibrio?
Explique detalladamente el procedimiento realizado
2.- Un dispositivo de cilindro-embolo contiene inicialmente un gas a 200 kPa y 30 ºC. En este estado, el embolo que tiene un diámetro de 5 cm, descansa sobre un par de topes, como se ilustra en la figura Nº 1, y el volumen encerrado es de 500 L. La masa del embolo es de 500 Kg. Si se calienta el gas hasta duplicar su volumen, determine
a) La temperatura final
b) El trabajo que realiza el gas
c) El calor total transferido al aire
Explique detalladamente el procedimiento realizado. -
Cual es el calor especifico del mercurio, si para elevar temperatura de 200 grados de eses material de 10 C a 30 C. Se necesitan entregar por calor 66 cal. de energía??
-
una pregunta
en el problema 6 porque o de donde salen los 720.225 gramos? -
¿Cuál es el calor específico de calcio si se necesitan 47.0 J para elevar la temperatura de 45.6 g de Ca a 14.6 °C? Exprese su respuesta en notación científica con tres cifras significativas, redondee si es necesario.
ayudenme
-
Resolver este problema
-
-
cuanto calor hay que suministrarle a 85g de un aceite ligero para que su temperatura aumente desde 25°c hasta 60°c . Ce (aceite)= 1800joule/g°c
-
Una consulta y que pasa cuando se tiene 2 sustancias en calentamiento ? Un sólido y un líquido ? Se suman los calores específicos ?
-
Resolver este problema
-
-
Por favor me ayudan..
1. ¿Cuál es el calor necesario para aumentar la temperatura de 25 gramos de vidrio desde 12°C hasta
23°C?2. ¿Cuál es la masa de un alambre de cobre que absorbe 234 calorías para aumentar su temperatura de
4°C hasta 18°C?3. ¿En cuánto varía la temperatura de 5 gramos de aire si al calentarse absorbe 155 calorías?
4. ¿Cuál es el calor específico de una sustancia desconocida, si 30 gramos de ella, absorben 115 calorías
cuando su temperatura aumenta de 20°C a 25°C?5. ¿Qué cantidad de calor absorbe una masa de 50 g de acero que pasa de 50 °C hasta 140 °C?
-
Quien me puede ayudar con esta??? Por favor
una sustancia de masa de 87,4g y un calor especifico de 0,077 cal/gc esta a la temperatura de 15,2 c calcula el calor necesario para que su temperatura alcance los 64,9-
Si no me equivoco es igual al problema 2, entonces sale 334,5 calorías (redondeado)
-
-
8 Litros de un líquido de densidad 0.86 gr/cm3 y calor específico 2.6 cal/g x °C están a la temperatura de 23 °C. Calcula el calor necesario para triplicar su temperatura.
-
Es un error de la edicion
-
Qué buena es esta página con ejercicios que los estudiantes podemos comprender. Muchas gracias!!!!
-
los felicito, es una muy buena página con una presentación muy atractiva y sobre todo información clara y concisa.
-
Bueno me sirvió para mucho muchas gracias
-
-
Gracias por despejar mis dudas bendiciones
-
Como que en la problema 2 la temperatura final es 95 y Los datos y la solucion se utilize 110?
-
en problema dos la temperatura final dice que es 110 grados pero en el problema dice que es 90??
-
de hecho la temperaturas que salen son 31 y 95, y en ninguna parte dice 110 no entiendo como sacarlo 🙁
-
El problema 2 está mal en los datos, la temperatura final es de 95, no de 110.
Aguas con sus respuestas -
si el ejercicio esta mal la cantidad de calor necesaria es de 86,016 cal
-
Sii está mal, a mí me dió 86,016cal
-
-
Una cuestión del problema N°2 la temperatura final en el escrito Dice 95°C y en el resolucionario se muestra con 110°C es un error o me podrían explicar el motivo por el cual cambió?
-
He muy bueno lo de usted pero por favor me podría ayudar con unos ejercicios donde explique la ecuación de calor y temperatura de los cuerpos
-
41 Deja tu comentario
Deja una respuesta

Estos temas te pueden interesar