Ley de Gay-Lussac - Ejercicios Resueltos

Qué hay amigos, hoy hablaremos sobre otra ley muy importante en los gases y que de manera resumida y muy práctica la vamos a ver durante este post, así que toma asiento, cuaderno, lapicero y calculadora en mano que es momento de aprender algo nuevo, y eso algo nuevo es ni nada más ni nada menos que sobre la ley de gay-lussac .
bien, hasta este momento en el blog tenemos dos leyes relacionadas entre si que dan paso a ley general del estado gaseoso que se verá en otro post, por ahora ya se ha comprendido de que trata la ley de charles y la ley de boyle-mariotte y si no las has revisado pues no esperes más, y dales una checadita.
Entendiendo la Ley de Gay-Lussac
Vamos a lo que nos importa e interesa, esta ley tiene una particularidad en general al igual que las demás, por ejemplo; en la ley de charles la presión permanece constante, en la ley de boyle-mariotte es la temperatura quien permanece constante y para finalizar en la la ley de Gay-Lussac es el volumen quien permanece constante.
Antes de meternos en las matemáticas y fórmula de gay-lussac, veremos algo más sobre esta ley.
Aquí entenderemos porque la presión y temperatura van muy de la mano y son totalmente proporcionales, es decir, supongamos que acabas de comprar un aerosol, si sometemos ese aerosol a cierta temperatura de tal manera que aumente, la presión también aumentará, a esta relación se le llama proporcionalidad.

Notables científicos, físicos y químicos dedicaron parte de su tiempo para poder entender mejor esta ley, pero fue Gay-Lussac un físico-químico de origen Francés, que estudió a fondo el comportamiento de los gases respecto a la relación entre la presión y la temperatura, su ley estable lo siguiente.
[su_box title="la Ley de Gay-Lussac dice:" box_color="#60a1c0" title_color="#ffffff" radius="2"]Si el volumen de una masa gaseosa permanece constante, la presión es directamente proporcional a su temperatura absoluta.[/su_box]
Ahora si, vamos a lo matemático.
Fórmula de Gay-Lussac
Como dijimos texto atrás, la proporcionalidad que existe en esta ley es sobre la presión y la temperatura, matemáticamente colocaremos esto como:
$\displaystyle P\propto T$
Ahora introduzcamos una constante de proporcionalidad esto da paso a que se vea de la siguiente forma, es como un despeje simple.
$\displaystyle \frac{P}{T}=k$
Ahora al tratarse de una igualdad, podemos considerar las condiciones inicial y final, quedando la ecuación o fórmula matemática de la Ley de Gay-Lussac de la siguiente forma:
$\displaystyle \frac{{{P}_{1}}}{{{T}_{1}}}=\frac{{{P}_{2}}}{{{T}_{2}}}$
donde:
$\displaystyle {{P}_{1}}=$ Presión Inicial
$\displaystyle {{T}_{1}}=$ Temperatura Inicial
$\displaystyle {{P}_{2}}=$ Presión Final
$\displaystyle {{T}_{2}}=$ Temperatura Final
Gráfica de la Ley de Gay-Lussac
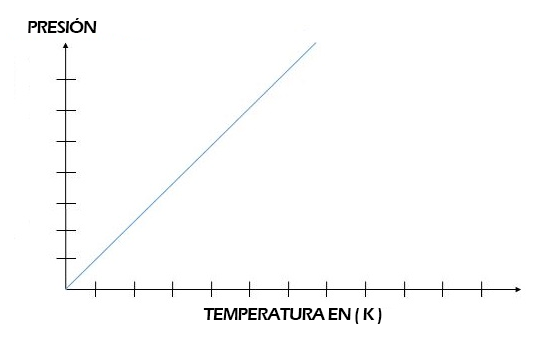
En la gráfica podremos observar claramente la proporcionalidad entre la presión y la temperatura, recordemos también que para las condiciones de un gas, las temperaturas deben darse en grados Kelvin.
Ejemplos resueltos de la Ley de Gay-Lussac
Solución: Si leemos detalladamente el problema nos podremos dar cuenta que las condiciones iniciales de temperatura y presión nos las dan como datos, al igual que la presión final, pero el único dato que no nos dan es la temperatura final, y la cual nos piden en °C.
Vamos a colocar nuestros datos:
$\displaystyle {{P}_{1}}=$ 440 mm de Hg.
$\displaystyle {{T}_{1}}=$ 35°C + 273 = 308 °K
$\displaystyle {{P}_{2}}=$ 760 mm de Hg.
$\displaystyle {{T}_{2}}=$ ?
He sumado a 35° la cantidad de 273, para poder hacer la conversión a grados Kelvin. Es muy importante que lo conviertan sino no dará el resultado que esperamos.
Ahora, usamos la fórmula para esta ley, la cual colocaré de nuevo.
$\displaystyle \frac{{{P}_{1}}}{{{T}_{1}}}=\frac{{{P}_{2}}}{{{T}_{2}}}$
Despejando a $\displaystyle {{T}_{2}}$
Nos queda
$\displaystyle {{T}_{2}}=\frac{{{P}_{2}}{{T}_{1}}}{{{P}_{1}}}$
Ahora sustituimos nuestros datos.
$\displaystyle {{T}_{2}}=\frac{(760mmdeHg)(308{}^\circ K)}{440mmdeHg}=532{}^\circ K$
Pero nos piden el resultado en °C, por lo que restaremos 273 a la cantidad resultante en grados Kelvin.
$\displaystyle {{T}_{2}}=532{}^\circ K-273=259{}^\circ C$
Como podemos observar en las condiciones iniciales del problema, la temperatura aumentó y como resultado también la presión, esto quiere decir que hemos resuelto el problema con éxito.
Veamos otro ejemplo:
[anuncio_b30 id=3]
Solución: Para este ejemplo podemos observar claramente que la variable que nos hace alta es la presión final, por lo que haremos una recopilación de nuestros datos y empezar a resolver.
Si hacemos el análisis también nos damos cuenta que la temperatura ha aumentado de 45°C a 125°C esto quiere decir que por la proporcionalidad que existe entre la presión y temperatura, la presión aumentará como resultado final, no sabemos en que cantidad, pero si sabemos que aumentará.
¡Muy importante! y vuelvo a repetirlo, la temperatura siempre será en escala absoluta, es decir grados Kelvin.
Datos:
$\displaystyle {{P}_{1}}=$ 460 mm de Hg.
$\displaystyle {{T}_{1}}=$ 45°C + 273 = 318 °K
$\displaystyle {{P}_{2}}=$ ?
$\displaystyle {{T}_{2}}=$ 125°C + 273 =398°K
Por fórmula tenemos
$\displaystyle \frac{{{P}_{1}}}{{{T}_{1}}}=\frac{{{P}_{2}}}{{{T}_{2}}}$
Despejando $\displaystyle {{P}_{2}}$
Nos queda
$\displaystyle {{P}_{2}}=\frac{{{P}_{1}}{{T}_{2}}}{{{T}_{1}}}$
Reemplazando nuestros datos en la fórmula
$\displaystyle {{P}_{2}}=\frac{(460mmdeHg)(398{}^\circ K)}{318{}^\circ K}=575.72mmdeHg$
Pero, para entenderlo mejor sigamos viendo un tercer ejemplo más 😎
Solución: Anotemos los datos de nuestro problema y veamos las variables que tenemos y la que nos hace falta, recordemos mantener a la temperatura en su escala absoluta, por lo que tenemos que convertir a Kelvin.
$\displaystyle {{P}_{1}}=2atm$
$\displaystyle {{T}_{1}}=27{}^\circ C$
$\displaystyle {{P}_{2}}=3atm$
$\displaystyle {{T}_{2}}=?$
Convertimos a la temperatura 1, en absoluta, quedando así:
$\displaystyle {{T}_{1}}=27+273=300{}^\circ K$
Ahora, nos damos cuenta que nos hace falta la temperatura final, o T2, por lo que procedemos a realizar el despeje de la fórmula.
$\displaystyle {{T}_{2}}=\frac{{{P}_{2}}{{T}_{1}}}{{{P}_{1}}}$
Sustituyendo en nuestros datos:
$\displaystyle {{T}_{2}}=\frac{{{P}_{2}}{{T}_{1}}}{{{P}_{1}}}=\frac{(3atm)(300{}^\circ K)}{2atm}=450{}^\circ K$
Por lo que la temperatura aumentó a 450°K, por lo que tiene lógica, ya que si vemos el aumento de la temperatura, se debe al aumento de la presión.
Solución: Nuevamente debemos recopilar nuestros datos, y a su vez recordar en convertir la temperatura que está en Celcius y pasarlas a Kelvin, así que aquí vamos.
$\displaystyle {{P}_{1}}=4atm$
$\displaystyle {{T}_{1}}={{47}^{{}^\circ }}C$
$\displaystyle {{P}_{2}}=?$
$\displaystyle {{T}_{2}}=127{}^\circ C$
Pasando a temperatura absoluta a nuestras temperaturas tenemos que:
$\displaystyle {{T}_{1}}=47+273=320{}^\circ K$
$\displaystyle {{T}_{2}}=127+273=400{}^\circ K$
Ahora despejamos de nuestra fórmula a la presión final o P2.
$\displaystyle {{P}_{2}}=\frac{{{P}_{1}}{{T}_{2}}}{{{T}_{1}}}=\frac{(4atm)(400{}^\circ K)}{320{}^\circ K}=5atm$
Por lo que la presión final es de 5 atmósferas ¿complicado?, seguro que no, no es complicado. Recuerda practicar y resolver más ejercicios para que aprendas de una vez por todas. 😎
Ejercicios para Practicar de Gay - Lussac
Resuelva los siguientes ejercicios y compruebe los resultados paso a paso haciendo click en la parte “ver solución”. ??
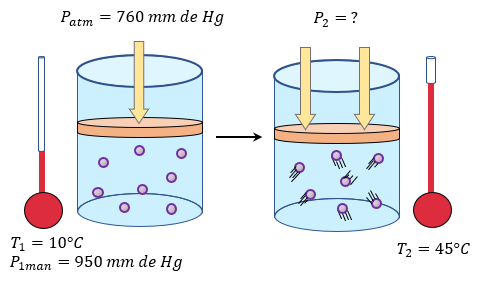
[alert-note] Problema 5. En un cilindro metálico se encuentra un gas que recibe una presión atmosférica de 760 mm de Hg, y cuando su temperatura es de 10°C , con el manómetro se registra una presión de 950 mm de Hg. Si al exponer el cilindro a la intemperie eleva su temperatura a 45°C debido a los rayos del sol, calcular:
a) ¿Cuál es la presión absoluta que tiene el gas encerrado en el tanque?
b) ¿Cuál es la presión manométrica?
[/alert-note]
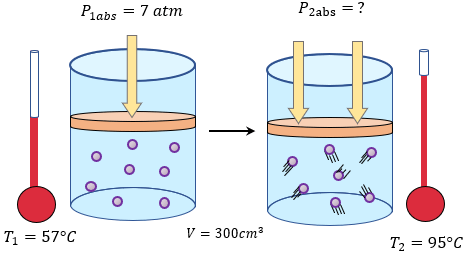
[alert-note] Problema 6. Una masa dada de gas en un recipiente recibe una presión absoluta de 7 atmósferas, su temperatura es de 57°C y ocupa un volumen de 300 cm³. Si el volumen del gas permanece constante y su temperatura aumenta a 95°C, ¿cuál será la presión absoluta del gas? [/alert-note]
Examen de la Ley de Gay-Lussac
Ahora es momento de demostar lo aprendido en el tema de Gay Lussac.
Cargando examen...
¿Te gustó este contenido?
Únete a nuestra comunidad en WhatsApp o Telegram para recibir nuevos proyectos, tutoriales y noticias exclusivas.
-
AGRADESCO QUE LEAS MIS COMENTARIOS
★★★★★
-
hola gracias por tu trabajo pero en la parte donde hay que cambiar Celsius a kelvin la formula exacta es:
°C + 273,15 no °C + 273 (solo para aclarar)
y el segundo error es que grados kelvin no lleva el símbolo grado ° debido a que K es una escala absoluta,entonces es:
K no °K
★★★★★
-
estoy es perando que contesten a sus aclaraciones el tien toda la razon
★★★★★
-
Supongo que es una aproximación, es muy común . Pero gracias por eso
★★★★★
-
-
muy buena la información de los diversos temas, y lo mejor es que presente ejercicios muy prácticos Felicitaciones.
-
un gas se encuentra en un recipiente cerrado, pasa de encontrarse a 15 atm de presión a 16 atm.¿cuál será la temperatura final dentro del recipiente si al principio se medían 25° c?
-
Me podrían explicar este ejercicio con la ley de gay lussac dadas 10l de gas carbónico a 4⁰C y 760mmhg determinada el volumen a 30⁰C y 800mmhg
-
Aquesta llei també és d'en Charles
-
Me podrían ayudar en este un gas a una temperatura de 35⁰C y a una presión de 440 mm de HG se calienta hasta que su presión sea de 1 atmósfera si el volumen permanece constante ¿cual es la temperatura final del gas en ⁰C
-
Por qué no viene el problema 3?
-
Se tiene un tanque de un compresor de 30 litros de 2 HP, se realiza un cambio del tanque
con una capacidad de 20 litros. ¿Cuáles son los efectos por cambio del tanque
manteniendo la misma potencia? -
una pregunta porque en ele ejercicio 3 queda en grado kelvin
-
Que año fue publicado este articulo
-
Hola tengo dudas en cuanto a un problema dice Un gas tiene una presión inicial de 15atm a una temperatura de 303ºk si al paso de 2horas su temperatura disminuyo a 273ºk ¿Cuál fue su presión final?.
Lo resolví usando la ley de GayLusacc y me salió como resultado final P2 13.51atm quiero saber si esta bien
-
hola me pueden ayudar plis con estos problemas
PI=1040MM HG
TI=?
P1=760MM HG
T2=0.0°C
PROBLEMA 2:
P1=?
T1=-10°C
P2=925MM HG
T2=308.5K -
Un estudiante lee en un recipiente que contiene gas metano la etiqueta con la siguiente información: Contiene 20
moles de gas a una presión de 3 atmósferas por lo que debe mantenerse a una temperatura de 50 grados Fahrenheit; Al
colocarlo en un barómetro para comprobar la presión, observa que marca 1,5 atmosferas, por lo que infiere que la
temperatura del recipiente debió haber subido y resuelve llevarlo a un refrigerador hasta que marque 2,5 centígrados.
Determine si hay errores por parte del estudiante en el proceso y de ser así haga las correcciones necesarias. -
hola, me puede proporcionar la fecha de cuando publico este trabajo?, necesito la fecha para mi trabajo, muchas gracias.
-
Hola una pregunta si por ejemplo el problema me dice Un tanque de acero de 200 L, contiene dióxido de carbono a 27° F y 5 atm.
¿Cuál será la presión interna del gas si se calienta hasta 100 °C?
Se que es la ley de Gay Lussac pero mi duda es que si el volumen tiene que ver o no lo tomo en cuenta, en cao de que si que formula se ocuparía?
Gracias por tu presentación -
si un problema tiene como datos: volumen, temperatura y presión. ¿se utiliza esta ley o cual ley tengo que aplicar?
-
Lo que has dicho es verdad sobre lo de la temperatura, pero y si en el resultado final pones la respuesta en grados Celsius cuando el problema te dicen que lo pases a Kelvin, en el resultado final podrías sumar el resultado en grados Celsius y sumarlo entre 273?
-
Hola soy Vicky, me pueden hacer el favor y me ayudan con esto...
una masa de nitrógeno confinada en un recipiente flexible a presión constante, permanece a una temperatura de 20 K con un volumen de 250 centímetros cúbicos.
¿Que le sucedera a su volumen si dicha temperatura empieza a aumentar?
Gracias!!! -
Hola tengo una duda si tengo un problema con una temperatura en negativo como quedaría al sumar los 273
"Una cierta cantidad de gas está contenida en un recipiente a -10°C y a 1 atm de presión. ¿Qué sucede si se aumenta la temperatura de este gas a 35°C sin modificar su volumen?
según yo quedaría en 263 k o estoy equivocado? -
carlos porfa es una nota muy importante.
-
Un gas con una presión inicial de 1,7 atmósferas a 78 grados centígrados, logrará enfriarse
A menos 22 grados centígrados cuál será su presión final. me ayudan porfabor es urgente es para hoy pliss -
tengo una pregunta en un ejercicio me da litros eso afecta a el proceso o no lo debo tomar en cuenta
-
2.-Una cierta cantidad de gas se encuentra a la presión de 790 mmHg cuando la temperatura es de 298,15 K. Determine la presión que alcanzará si la temperatura sube hasta los 473,15 K, si el volumen se mantiene constante.
-
ayúdenme con esta porfa
1. La presión ejercida por el gas H2S a 28 ºC es de 625 torr. ¿Cuál es su presión en mmHg a 80 ºC si el volumen permanece constante? (Recuerde que 1torr es igual a 1 mmHg) -
alguien tendrá la respuesta de este ejercicio me arian un gran favor una llanta de automóvil es inflada a una presión mano métrica de 28 lb/in2 en un momento en que la presión ambiental es de 14.4 lb/in2 y la temperatura es de 70 °f. después de conducir la temperatura del aire aumenta a 100 °f. si se supone que el volumen es constante, ¿cuál será la nueva presión mano métrica en la llanta?
-
Un gas que está a una temperatura de 27 ºC, triplica su presión a volumen constante.¿Cuánto valdrá en ese momento su temperatura en grados centígrados? (porfa :´()
-
Un gas encerrado en un recipiente mantiene una temperatura inicial de tu No. de Equipo grados Celsius y tiene una presión manométrica inicial de 2.1 atmósferas. ¿Cuál es la temperatura del gas en grados Celsius, si su presión manométrica es de 1,748 Torr? Se considera presión atmosférica como 1 ATM
-
ayudame con este ,
Una esfera aislante de radio R1=5cm tiene carga neta de +3Q. Esta esfera está situada en el
interior de otra esfera hueca conductora con radios interior y exterior R2=7cm y R3=8cm,
respectivamente y tiene una carga neta de +5Q. Cuál es le valor del campo eléctrico en las zonas
1 y 4 -
solo una pequeña ayudita.
Que volumen ocupa a 60°c cierta masa gaseosa que a 0°c tiene un volumen de 80 litros, considerando la presión constante-
Me ha salido esta también y me he encontrado con que todo se divide por 0 jajaja ... o sea será volumen indefinido
-
-
ayedeme una masa de nitrogeno ocupa 5 litrosbajo una precion de 714 milimetros de mercurio.determina el volumen de la misma masa de un gas a precion normal esto es a 760 mmhg permanece constante la
temperatura -
en el ejercicio seis sale 7.806 no 7.606
-
muy buena pagina me ha ayudado mucho
saludos -
Hola Carlos podrias ayudarme a resolver este ejercicio por favor :
En un tanque se almacenan 20 litros de oxígeno a la presión de 2 atmósferas, es necesario transportarlo desde un lugar que tiene una temperatura de -10°C, hasta otro de 30°C. ¿Qué presión en mm de Hg debe soportar el tanque? -
Hola plis me pueden ayudar con este ejercicio 1 La rueda de un coche contiene aire a una presión de 2,5 atm y la temperatura es de 20ºC. Después
de un largo recorrido la temperatura del aire asciende hasta 50ºC.¿Qué presión tendrá el aire de la
rueda? Solución: 2,75 atm
6. Un gasGracias de antemano
-
Hola me podrias ayudar, Una moto viaja por la autopista al iniciar el viaje las llantas marcaban una presion de 28 psi. ¿A cuantos °C se encontraran las llantas?
Segun entiendo la presion seria lo mismo que la temperatura, serian 28 kelvin? y luego los convierto a centigrados? estoy super perdida ayudame porfitas -
Como agositengo 45.17lb/pulgadas
-
Alguien que me pueda ayudar a resolver este problema con la ley de Gay-Lussac.
En un bulbo cerrado de vidrio, se puso helio a 750 mm hg y 27°C, el bulbo se rodeo de helio seco hasta bajar la temperatura a -73°C. ¿Qué presión estará ejerciendo el helio? -
Hola a mi lo que se me complica es como sabemos a que ley pertenece
-
y si me esta pidiendo el volumen, como lo puedo hacer?
-
Per nosotros tenemos que P1/T1=P2/T2 es la ley de Amonton no de Gay lussac
-
un gas ocupa un volumen de 87.0 ml a 27°C y 740 torr ¿Que volumen en ml ocupara el gas a 5°C y 740 torr?
-
Hola, solo quería dar las gracias por la ayuda que me has dado, estos ejercicios me están sirviendo de mucho para recuperar Física y Química, aunque aún no he hecho el examen, gracias a estos ejercicios voy mejorando poco a poco. ¡Resultas hasta mejor que un profesor particular!
Att:
Claudia.
-
Y desde ya muchas gracias
-
Hola soy de secundaria de segundo año podrias darme un ejemplo no tan avanzado por favor
Me encanto todo muy buena info. -
hola, podrías ayudarme con este problema por favor?
un recipiente sellado e indeformable de oxigeno se encuentra a 80°C con una presión de 2500 KPa, si se sumerge en agua con hielo (0°C), ¿cuanto baja la presión del oxigeno cuando llegue a 0°C?
gracias -
Hola, me parece muy bueno este articulo pero me parece que le falta un signo de interrogación en el segundo problema.
-
Gracias a este artículo entiendo las leyes, muchas gracias Carlos Julián
-
Un favor, no le entiendo a un problema que mi profesor nos puso de tarea, yo siento que está mal redactado....
Un gas contenido en un recipiente está a una presión de 0.70 atm a 90°F, si la presión cambia a 35mmHg ¿Cual será su presión en Kg/cm2?
No le entiendo, me da solo una temperatura y dos presiones, y todavía me pide presion, aiudaa :c
-
Hola disculpe , pero tengo una pregunta y prisa también . ya que estoy en exámen único y es de este tema, aún no comprendo bien porque hay dos fórmulas para la misma ley p1xt2=p2xt1 y la otra es
P1 = T2
P2. T1
Y porque en algunos ejercicios no se suma ( 273k y en otros si ) y que tengo que saber para reconocerlo
Agradecería su pronta respuesta :3 -
hola! me llama la atención que utilizando está ecuación de gay-lussac P= k. T no me de los mismo resultados con la ecuación que propones. Pensé que con los datos iniciales podía obtener la constante y con ellos poder obtener la temperatura final y resolviendo el ejercicio, no me daba y ahora q te leo, lo hice como propones si que me da bien. A diferencia de la ley de boyle que si me sale cuando busco K para buscar un dato final.
-
Muchas gracias por la explicación! ????
Saluditos! ?? -
Maestro Carlos, gracias por su página, la cual me ayudó mucho con mi tarea, Saludos Virginia
-
Hola me podrías ayudar no se si estoy bien en mi experimento ya que estoy muy confundida mira hice también la botella con el globo escogi la ley gay-lussac
según yo la botella es de 600 ml la temperatura del agua seria 20°C el agua caliente sería de 300°c para que se infle el globo la verdad no se como poner mis datos para hacer las operaciones ya que tengo que sumar los kelvins y despues despejar eso si se hacerlo lo unico que me falta hacer es que me ayuden a poner los datos porque en vi en alguanas paginas que tengo que llegar a 760mmHg no se si tengo que ocupar ese dato ayuda voy hacer un proyecto y la verad que no se -
Me podrias ayudar con este problema
Un gas en un recipiente de 2L a 293k y 560 mmhg ¿A que temperatura en grados centigrados llegara el gas si aumenta la presion interna hasta 760 mmhg -
Hola Carlos Gracias gracias me ayudaste a estudiar para mi prueba no entendia mucho esta ley...
te pasaste eres un CRACK 😉 -
Hola me podrias ayudar con este ejercicio no le entiendo muy bien.
22 litros de cloro se encuentra a una temperatura de 42 °C. Cual será la temperatura del gas si el volumen ha aumentado a 35 litros? -
No lo entiendo
-
cual seria la formula para sacar la presion absoluta y la presion manometrica?
tengo los sig datos:
P1=760mm de Hg
T1=289°k
P2=1650mmde Hg
T2=318°k -
HOLA; no entiendo nada de la Ley de Gay Lussac,
podrías ayudarme con este problema de dilatación
una varilla de aluminio es 0.239% mas larga a 100°C que a o°C
Si se construyera un termómetro con esa varilla de aluminio y se hiciera una extrapolación líneal al punto de longitud 0
¿a qué temperatura se llegaría a la desaparición de la varilla?
para esto debo utilizar V final = V inicial [1+alfa(t final-t inicial)gracias
-
Hola, tengo una pregunta, ¿Donde puedo conseguir más de estos ejercicios/ejemplos, necesito más de estos, es URGENTE
-
Hola, tengo una duda. Me dan este problema: Si un tanque de oxigeno se somete a una presión de 3atm con una temperatura de 20ºC, ¿Qué temperatura se necesitará para someterla a una presión de 3420 Torr? No entiendo 🙁 ¿Me ayudas por favor?
-
explicas muy bien
-
hola guapo
-
hola oye mira nose si me puedas ayudar con unos problemas que la verdad no entiendo
1-un compresor de aire a 2m|3 (cubicos) de aire a 20°C y la precion de una atmosfera (101.3 KPa).si el compresor descarga enn un deposito de 0.3cm|3 a una precion absoluta de 1500KPa ¿cual e sla temperatura del aire descargado? -
gracias por su ayuda
-
hola me podrias orientar en este problema k presion aguanta un globo lleno de aire k se calienta a 30° c ,cuando esta lleno de aire en condiciones normales de presion y temperaura
-
Hola como seria para despejar...p2 y T2
-
Hola. En la ley de Gay- Lussac, si la presion se da en mm de Hg, hay que pasarla a atm???
-
Hola dame 5 ejemplos de la ley de gay-lussac pls
-
hola tenia una pregunta. segun lo que me dieron a mi tengo volumen y temperatura.Se resuelve igual que estos nada mas que cambiando la prsion por volumen o se hace distinto?
-
enhorabuena Carlos me ha venido muy bien para estudiar graciaaas
-
disculpa buenas tardes me podria ayudar con 3 ejercicios de gay lusacc
-
hola profesor, gracias por los cursos de fisimat la verdad no entendia muy bien las leyes de los gases se me hacia muy complicado pero ahora las estoy entendiendo mejor .
-
Carlos Julián exelente contenido entendi super bien ¿eres profesor¿
-
Hola Carlos Julián
A mi me solicitaron realizar un experimento basado en cualquier ley de los gases, yo seleccione la ley de Gay Lussac utilizando un globo, botella de plástico y agua hirviendo, cuando vacío el agua hirviendo a la botella y coloco el globo en la boquilla de la botella de plástico y agito la botella, el globo se infla, pero en mi ejercicio me pide que ponga formula y si es necesario un procedimiento la formula para esto estoy confundida ellos dicen que la formula debe de ser V1/T1= V2/T2 yo digo que debe de ser P1/T1= P2/T2
no se cual deba de usar, de las dos y como puedo realizar el ejercicio matemático si no tengo las temperaturas ni la presión, o el volumen -
Temperatura (°K) Presión (Pa)
293.15
Tengo esta temperatura necesito saber cual es su presión me puedes ayudar -
cabe de mencionar carlos julian que admiro esa dedicación de contestar cada duda sobre estas leyes sigue asi (Y)
-
Hola Carlos Julian
Ya hiciero esta pregunta, sin embargo aún no lo comprendo.
Se tienen problemas en los cuales esta muy claro sobre las temperaturas, °C y las absoluta k, me perturaba sobre la presión, en algunos enunciados dan una presión en P, lb sobre pulgada cuadra, en atmosferas.
Se toma como la absoluta?
No se tiene duda cuando nos dan la manométrica.
Gracias por tus atenciones. -
En este caso Carlos, con ley de Gay, que tan cierto es que a la hora de sustituir después del despeje yo voy a modificar la fórmula o existen unas formulas... Me las puedes dar por favor.
-
Hola,Carlos mira, que no pasa nada si por ejemplo cambiamos de orden como en el primero así 440 mm de Hg por 308 kelvin entre 760 mm de hg
-
No entiendo Aicha! ¿a qué te refieres?
-
-
Hola en el ejercico 2 a mi me da 568,49 y eh multiplicado y dividido lo mismo q husted. Si me puede explicarlo gracias.
-
disculpa desconozco un poco sobre el tema de donde sale el resultado final?
-
Hola! tengo una duda (tal vez muy tonta)porque en el segundo problema ya no le restaste los 273?. segun yo, pues porque es necesario sumarle 273 a 45°C Y a los 125°C para poder sacar la presion ya que es lo que pide o no? porfa sacame de esa duda.
Saludos. -
OLA CARLOS ME PUEDES AYUDAR EN UNOS EJERCICIOS DE LA LEY DE GAY LUSSAC
POR FAVOR.
LA SEMANA QUE VIENE TENGO APORTE DE TODAS LAS LEY
LEY DE BOYLE
LEY DE CHARLES
Y
LA LEY DE GAY LUSSAC -
OLA ME PUEDES AYUDAR CON ESTO XFV
CUAL ES LA TEMPERATURA EN LA CUAL SE HAYA 12 MOLES DE MOLECULAS DE UN GAS SOMETIDAS A 4 ATMOSFERAS DE PRESION EN UN RECIPIENTE DE 21 LITROS
-
hola.me pueden ayudar ..dice que realizar la grafica de gay lussac si la temperatura cambia a 90ºc 250ºC 400ºC y 620 ºC
-
hola preciso ayuda con el siguiente problema:
me dice que realize un gráfico de presion en funcion del volumen a temperatura constante
experiencia 1: presión 5: volumen12 -
hola. mi pregunta no es acerca del ejercicio en si, es algo,pasa que me piden graficar y resolver,pero no entiendo que
graficas debo hacer para estos casos de ejercicios.gracias. -
ok.. 😉
-
Hola... disculpa tengo una duda.. me parece que la gráfica esta errada, pues corresponde a la ley de Charles y no a la de Gay- Lussac.. porque la relación directamente proporcional se da es entre la presión y la temperatura a volumen constante..
-
muy buena explicación esta semana será la prueba espero no me balla mal pero con tu pagina imposible saludos aah y de pais eres
-
carlos pero para sacar a grados centigrados otra vez debes aplicar la formula de 5/9(K-32) no se puedes restar 273 porque varia la respuesta es 277.7
-
hay no estoy confundido jajaj sorry jajaj
-
-
experiencia?
-
y para sacar P2?
-
Hola CArlos como resuelvo hallar la presion atm de un gas a 50ºC y un volumen de 9,5 cm3
-
Por fa necesito 15 de la ley de gay lusacc ayudame para no quedarmee!
-
se ..escribe en grados kelvin porque los gases se miden en grados kelvin......solo el problema es formulado en grados centigrados..
-
Disculpe cuantos años tiene esta ley???
-
buenaas por que ahi que sumarle 273 a la temperatura ?
-
Y CUAL ES LA FORMULA PARA QUE NOS SALGA P1 O T1????
-
entonces todo se maneja con kelvin y la presion dada pero no entiendo por que mi maestra me hacia convertir pascales a atm
-
Hola Carlos , hace falta pasar a KELVIN los grados también en la ley de BOYLE?
-
Hace falta pasarlo todo a K aunque no sea esta formula,me refiero si es laley de Charles también?
-
me ayudas en este problema porfavor
>El manometro de un tanque de oxigeno registra una presion de 30kpa a una t=35ªc ¿cuales son la temperatura y la presion absoleta del gas?bueno segun yo hice esto pero ya no se que mas hacer
primero convertir los ºc a kelvin que me da 308kdespues (que no se si estoy bien o estoy mal ) hice una conversion de 30kpa a precion atm entonces
me da = 0.29607 atmentonces segun la formula para encontrar la presion absoluta del gas es : pabs = pmano + patmo : es aqui donde tambien tengo una duda .... se sumanlos 30kpa? + la presion atm? si es asi entonces me da = 30.29607 pabs
bueno si es asi que estoy bien entonces para hacer lo siguien para encontrar la temperatura que hago? mi presion 2 seria esa? = 30.29607 o como? es donde no entiendo 🙁
-
a mi tambien me encargaron ese problema, en el tec de xalapa y no pude
-
si pudiste? por que yo si pude.. soy marcos
-
-
presion atm vale 1 y la presion manometrica de 30kpa vale .29 entonces las sumas y te da presion abs osea 1.29 atm
-
-
¿cuando la presión es absoluta o atmosférica,la formula es la misma?
-
por que as convertido los grados C a K, si los a pedido en el ejercicio en C desde un principio y la temperatura 1 también es en C ?
-
Por que si no resolvemos a kelvin no se puede obtener el resultado que se espera
-
Hola, el ejercicio 6 esta malo, ya que 95°C+273=368K
-
Porque siempre para resolver se debe transformar primero a k, es como una regla que siempre debes aplicar, si haces en C directo veras que te va a salir otra respuesta que ni siquiera se va a aproximar a la original
-
me ayudas por favor mi ejercicio es sobre la ley de gay-Lussac si la temperatura aumenta 473 k ¿ cual es la presión
-
faltan datos
-
-
-
Porque cuando habla de temperatura en la ley de volumen constante hay que sumarle 273,15 para pasarlo a grados kelvin y después restárselo porque te lo pide en grados centígrados.
-
porque siempre hay que darlo en kelvin
-
175 Deja tu comentario
Deja una respuesta

Estos temas te pueden interesar