Ley de Boyle-Mariotte - Ejercicios Resueltos
Bien, bien! Hoy hablaremos sobre la ✅ ley de Boyle-Mariotte, y como siempre no me pondré hablar mucha la teoría porque entiendo que como estudiante lo que más detestamos es enrollarnos mucho con ello, y preferimos siempre la forma práctica. Es por ello que en este post, haré mención de como podemos enfrentarnos con esta famosa ley.
Antes que nada quiero decirte y hacerte entender que Boyle y Mariotte son dos científicos distintos, uno Irlandés y el otro Francés respectivamente, lo que quiero es que no vayas a pensar que esto se trate de una sola persona. Así que sabiendo esto, y con respeto a estos dos grandes científicos daremos inicio a el desglose del tema.
Entendiendo la ley de Boyle Mariotte
El comportamiento de un gas va depender siempre de la relación que existan entre tres factores muy importantes, que son: el volumen, la presión y la temperatura. No obstante, estas relaciones fueron experimentadas por los científicos Boyle y Mariotte, de tal forma que dicho principio se generaliza como:
Si la temperatura permanece constante, el volumen de una masa gaseosa es inversamente proporcional a la presión que se le aplica.
Es muy probable que al leer el enunciado citado arriba, no lo entiendas del todo, y te doy la razón, está confuso en principio, pero aquí te diré que nos quiere dar a entender.
Vamos a establecer matemáticamente el enunciado.
$\displaystyle V\propto \frac{1}{P}$
Despejando, de tal forma que nos quede la unidad en el miembro derecho, tendremos algo así.
$\displaystyle PV\propto 1$
Introduciendo la constante de proporcionalidad, nos queda que:
$\displaystyle PV=K$
Ahora, si queremos ver los cambios que experimentará un gas, comúnmente se hace en un estado inicial y final, por lo que la expresión matemática o fórmula de Boyle-Mariotte queda de la siguiente forma.
$\displaystyle {{P}_{1}}{{V}_{1}}={{P}_{2}}{{V}_{2}}$
Dónde
$\displaystyle {{P}_{1}}=$ Presión inicial
$\displaystyle {{V}_{1}}=$ Volumen Inicial
$\displaystyle {{P}_{2}}=$ Presión Final
$\displaystyle {{V}_{2}}=$ Volumen Final
[alert-warning]En pocas palabras la Ley de Boyle- Mariotte nos quiere dar a entender que si la presión aumenta, el volumen disminuye, y si la presión disminuye el volumen aumenta. Fácil ¿no?? [/alert-warning]
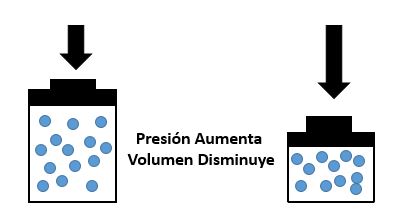
Fórmula de la Ley de Boyle - Mariotte
En resumen, para la resolución de problemas de este tipo de ley, usaremos la fórmula:
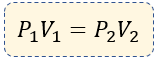
Ejemplos resueltos de la ley de Boyle-Mariotte
Solución:
Lo primero que vamos analizar para la resolución del problema, son nuestros datos, saber que tenemos y que nos hace falta.
$\displaystyle {{V}_{1}}=$ 4.2 litros
$\displaystyle {{P}_{1}}=$ 760 mm de Hg.
$\displaystyle {{P}_{2}}=$ 415 mm de Hg.
$\displaystyle {{V}_{2}}=$ ?
Por lo que podemos observar el problema nos pide el volumen final es decir $ \displaystyle {{P}_{2}}=$ , vamos a utilizar la fórmula de Boyle-Mariotte e iniciaremos a despejar la variable que necesitamos para poder iniciar a resolver el problema.
$\displaystyle {{P}_{1}}{{V}_{1}}={{P}_{2}}{{V}_{2}}$
Despejando >> $\displaystyle {{V}_{2}}$
$\displaystyle {{V}_{2}}=\frac{{{P}_{1}}{{V}_{1}}}{{{P}_{2}}}$
Sustituyendo nuestros datos.
$\displaystyle {{V}_{2}}=\frac{(760mmHg)(4.2l)}{415mmHg}=\frac{3192}{415}l=7.69l$
Por lo que nuestro volumen final es de $ \displaystyle 7.69$ litros.
Con esto podemos concluir que mientras la presión bajó el volumen aumentó.
No es difícil analizar dichos problemas, veamos otro ejemplo.
Solución:
Al igual que el problema anterior lo que necesitamos es conocer nuestros datos, sin los datos no podemos hacer absolutamente nada, ahora hagamos de nuevo un listado de nuestros datos.
$\displaystyle {{V}_{1}}=$ 1.5 litros
$\displaystyle {{P}_{1}}=$ 2.5 atm.
$\displaystyle {{P}_{2}}=$ ?
$\displaystyle {{V}_{2}}=$ 3 l
Observamos que lo que nos falta es la presión final, por lo que vamos a despejar $ \displaystyle {{P}_{2}}$ de la fórmula.
$\displaystyle {{P}_{1}}{{V}_{1}}={{P}_{2}}{{V}_{2}}$
Despejando >> $\displaystyle {{P}_{2}}$
$\displaystyle {{P}_{2}}=\frac{{{P}_{1}}{{V}_{1}}}{{{V}_{2}}}$
Sustituyendo nuestros datos.
$\displaystyle {{P}_{2}}=\frac{(2.5atm)(1.5l)}{3l}=\frac{3.75}{3}atm=1.25atm$
Tenemos que 1.25 atm. es la presión final de lo que nos pide nuestro problema, sin embargo el mismo problema dice que tenemos que convertir las unidades de presión, en este caso atmósferas a mm de Hg para ello haremos una regla de tres.
Si 1 atm equivale a 760 mm de Hg, 1.25 atm ¿a cuántos mm de Hg equivaldría?
1 atm ----------- 760 mm de Hg
1.25 atm ------------ x mm de Hg
$\displaystyle x=\frac{(760mmdeHg)(1.25atm)}{1atm}=950mmdeHg$
por lo que 950 mm de Hg es la presión final obtenida en un recipiente de 3 litros.
¿Aún no quedó claro?
Ejercicios para Practicar de la Ley de Boyle Mariotte
Para aprender mucho mejor el tema de la Ley de Boyle - Mariotte, es importante resolver más ejercicios y comprender los problemas para entender que variable tenemos que despejar y poder resolver sin ningún problema. Los siguientes ejercicios son explicados paso a paso en su solución, pero primero resuélvalos usted en su cuaderno o libreta. ??
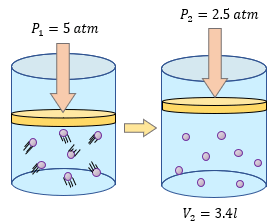
[alert-note]Problema 3.- Calcular el volumen de un gas a una temperatura constante al recibir una presión de 5 atm, si su volumen es de 3.4 litros a una presión de 2.5 atmósferas. [/alert-note]
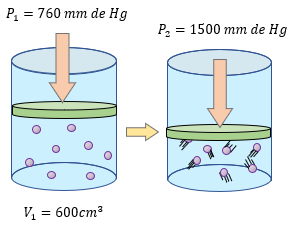
[alert-note]Problema 4.- Un gas a una temperatura constante ocupa un volumen de 600 cm³ a una presión de 760 mm de Hg, ¿cuál será su volumen si la presión recibida aumenta a 1500 mm de Hg? [/alert-note]
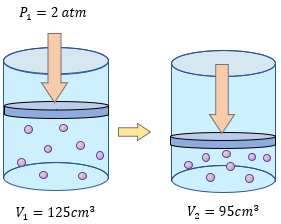
[alert-note]Problema 5.- Un gas recibe una presión de 2 atmósferas y ocupa un volumen de 125 cm³, calcular la presión que debe soportar para que su volumen sea de 95 cm³ [/alert-note]
Examen de la Ley de Boyle - Mariotte
Ahora es momento de practicar tanto la teoría como la práctica, ¿estás listo/a?
Cargando examen...
¿Te gustó este contenido?
Únete a nuestra comunidad en WhatsApp o Telegram para recibir nuevos proyectos, tutoriales y noticias exclusivas.
-
:3 muy bueno mi mama me iva a pegar XD
-
Hola Sr. Carlos Julián me podria ayudar con el siguiente ejercicio por favor que no tengo idea como hacerlo se lo agradezco mucho: 1. Una muestra de un Gas a 27°C de temperatura y Presión de 1atm que ocupa un Volumen de 0,4 Litros, se calienta hasta una Temperatura de 177°C, incrementandose su volumen hasta 0,5 Litros ¿Qué Presión ejercerá ahora?
-
estimado la precion q ejercera sera de 1.2 atm
-
considero que aquí si se puede aplicar la ley de Boyle-Mariotte porque están preguntando su presión 2, quedando la solución de la siguiente manera:
recordando la formula: V1 P1= V2 P2
V1= 0,4 litros
P1= 1 atm
v2=0,5 litros
p2=?si despejamos
P2= (V1X P1)/ V2Reemplazando
P2= (0,4 litros x 1 atm) / 0.5 litros = 0.8 atm ( ya que la unidad de litros que multiplica con el que divide se cancelan quedando la unidad de respuesta en este caso atm.RTA: la presión que ejercerá ahora es de 0.8 atm
-
Tres litros de CO2 esta a una presion 1 atm ¿ Que volumen ocupa este gas cuando la presion aumenta dos atmosferas
-
-
el segundo problema no esta bien la respuesta en mm de Hg es 912
-
Piensa antes de escribir.
Si te da: 1,25 atm x 760 mmHg, te dará: 950 mmHg
-
-
y como seria para sacar p1 o v1??
-
No se baja saludos
-
-
Eres un crack me loe aprendido gracias ti
-
Esta fácil, gracias me salvo de una exposición
-
• Qué masa de cloruro de hidrógeno gas se necesita para ejercer una presión de 24.3 kPa (Pa= Pascal) en un recipiente de 250 mL a 37C? Datos masas atómicas: H=1, Cl=35.5
-
Una masa de nitrogeno ocupa 5 litros bajo una presion de 740mm hg.determina el volumen de la misma masa de gas a una presion de 760 mm hg
-
-
149 Deja tu comentario
Deja una respuesta

Estos temas te pueden interesar